დარიშხანი
დარიშხანი - As (Arsenicum) ქიმიური ელემენტია ატომური ნომრით 33. დარიშხანი ძლიერი საწამლავია. იგი არსებობს მრავალი ალოტროპიული სახით, თუმცა მხოლოდ მისი რუხი ფორმაა მნიშვნელოვანი. დარიშხანი და მისი ნაერთები ძირითადად გამოიყენება, როგორც შემალღობელი აგენტი ტყვიის ბატარეებში, მაგრამ ისტორიულად იგი ფართოდ გამოიყენებოდა, როგორც პესტიციდი, ჰერბიციდი, ინსექტიციდი, თუმცა ამ მიმართულებით მისი გამოყენება თანდათან მცირდება. მსოფლიოს ზოგიერთ ნაწილში დარიშხანის არსებობა სასმელ წყლებში პრობლემატურია.

ბუნებრივი დარიშხანი
გავრცელება
მინერალური ფორმულით MAsS და MAs2 (M = Fe, Ni, Co), წარმოადგენს დარიშხანთან ერთად დარიშხანის კომერციულ წყაროს. ამის ილუსტრაციას წარმოადგენს არსენოპირიტი (FeAsS), რომელიც სტრუქტურულად ჰგავს რკინის პირიტს. გარდა ამისა, ცნობილია ბევრი დარიშხანშემცველი მინერალი.
ზემოთ მოყვანილი არაორგანული ფორმების გარდა დარიშხანი ჩვენს ირგვლივ აგრეთვე გვხვდება ორგანული ფორმებითაც. სხვა ბუნებრივი ფორმები გვხვდება ვულკანურ ფერფლში, აგრეთვე დარიშხანის შემცველ მინერალებში და ნიადაგის წყლებში. იგი აღმოჩენილია საკვებში, წყალში, მტვერში და ჰაერში.
2005 წელს ჩინეთი აწარმოებდა თეთრი დარიშხანის მსოფლიო წარმოების 50%-ს, შემდეგ იყო ჩილე, პერუ და მაროკო.
ისტორია

რეალგარი
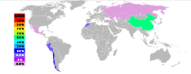
დარიშხანის მოპოვება 2006 წელს
სიტყვა ”arsenic” წარმოდგება სირიული სიტყვისგან ”zarniqa” და სპარსული სიტყვისგან ”Zarnikh” რაც ნიშნავს ”yellow or pigment” (პეროპიგმენტი As2S3) – ბერძნულად ”arsenikom”. იგი აგრეთვე ენათესავება ბერძნულ სიტყვას ”arsenikos” , რაც ნიშნავს "masculine" ან "potent" (ძლიერს). ეს სიტყვა აგრეთვე ენათესავება ლათინურ ”arsenicum” - ს და ძველ ფრანგულ ”arsenic” , რომლისგანაც წარმოდგა ინგლისური სიტყვა ”arsenic” - დარიშხანი. დარიშხანის ბუნებრივი ნაერთები ოქროსფერი-მოყვითალო პეროპიგმენტი As2S3 და მუქი ყავისფერი რეალგარი As4S4 ჯერ კიდევ უძველესი ხალხისთვის იყო ცნობილი, რომლებიც ამ მინერალს იყენებდნენ საღებრების და წამლების დასამზადებლად.
ბრინჯაოს ხანაში დარიშხანი ხშირად გაიგივებული იყო ბრინჯაოსთან, მისგან მიღებული შენადნობები იყო მძიმე (ე.წ “arsenical bronze”) ა.მაგნუსმა პირველად გამოყო ელემენტი დარიშხანი 1250 წ-ს საპნის დარიშხანის ტრისულფიდთან გაცხელებით. 1643 წ ჯ. შროდერმა გამოაქვეყნა დარიშხანის მიღების ორი გზა. ლ. გასიქორდის მიერ 1760 წ სინთეზირებული იქნა პირველი სინთეზური მეტალორგანული ნაერთი კალიუმის აცეტატისა და დარიშხანის ტრიოქსიდის ურთიერთქმედებით.
XVIII საუკუნის მეორე ნახევარში “arsenic” ( დარიშხანის თეთრი ტრიოქსიდი) შეურიეს ძმართან და ცარცთან და ამით იკვებებოდნენ ქალები სახის ფერის გასაუმჯობესებლად. ”arsenic”-ს ქალები იყენებდნენ აგრეთვე სახისა და მკლავების შესაზელად, მაგრამ ”arsenic” - ის საკვებზე დამატებამ 1858 წ გამოიწვია მოწამვლა და დაახლოებით 20 ადამიანი დაიღუპა.
იზოტოპები
დარიშხანის სტაბილური იზოტოპი, რომელიც გვხვდება ბუნებაში არის 75As. 2003 წლისათვის სინთეზირებული იყო 33 რადიოიზოტიპი, ატომური მასით 60-დან 92-მდე. ამათგან ყველაზე სტაბილურია 73As ნახევარდაშლის პერიოდით 80.3 დღე. უახლოეს პერიოდში აღწერილ იქნა 10 ბირთვული იზოტოპი ატომური მასით 66-დან 84-მდე. ამათგან ყველაზე სტაბილურია მეტა68As ნახევარდაშლის პერიოდით 111 წმ.
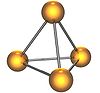
ყვითელი დარიშხანის As4 სტრუქტურა
ფიზიკური თვისებები
დარიშხანის ალოტროპიებს შორის მისი ლითონური რუხი ფორმა ყველაზე მნიშვნელოვანია. მისი სტრუქტურა გრაფიტის (შრეებად განლაგებული) მსგავსია და შეიცავს ექვსწევრიან ბირთვებს. თითოეული ატომი ფენებში უკავშირდება სამ სხვა ატომს და კოორდინირებულია დარიშხანის სამი ატომით. მას გააჩნია მაღალი სიმკვრივე - 5.73გ/სმ3. იგი ნახევარგამტარია და რბილი (მოხის სკალით 3.5).
დარიშხანს, ფოსფორიდის მსგავსად ახასიათებს ალოტროპია. ცნობილია სამი ალოტროპიული სახესხვაობა: მეტალური რუხი, ყვითელი და შავი დარიშხანი. ყვითელი დარიშხანი (As4) რბილი და ცვილისებურია, იგი რამდენადმე ემსგავსება P4-ის მოლეკულებს. ორივე ნაერთში ოთხი ატომი განლაგებულია ტეტრაედრულად. სტრუქტურაში, რომელშიც თითოეული ატომი დარიშხანის ერთმაგი ბმით უკავშირდება დანარჩენ სამ ატომს. ეს არამდგრადი ალოტროპი მოლეკულურია, ძლიერ აქროლადი და აქვს დაბალი სიმკვრივე, ძლიერ ტოქსიკურია. ყვითელი დარიშხანი (სიმკვრივე - 1.97 გ/სმ3 ) მიიღება დარიშხანის ორთქლის თხევად აზოტში სწრაფი გაცივებით, იგი სინათლის მოქმედებით სწრაფად გადადის რუხ დარიშხანში.
შავი დარიშხანი სტრუქტურით წითელი ფოსფორის მსგავსია. დარიშხანის სამი მეტალოიდური სხვადასხვა სტრუქტურის ფორმები თავისუფალი სახით ნაპოვნია ბუნებაში.
ქიმიური თვისებები
დარიშხანი ტრიოქსიდამდე იჟანგება ჰაერზე გაცხელებით. ამ რეაქციის დროს იგრძნობა ნივრის სუნი. ასეთივე სუნი იგრძნობა მინერალ არსენიდის - არსენოპირიტის ჩაქუჩით დამტვრევის დროს. დარიშხანი (და მისი ზოგიერთი ნაერთი) გაცხელებით სუბლიმირდება ატმოსფერულ წნევაზე. თხევად მდგომარეობაში გადადის 20 ატმოსფეროზე და ზევით. ამით შეიძლება აიხსნას, თუ რატომაა მისი ლღობის ტემპერატურა უფრო მაღალი, ვიდრე დუღილისა.
დარიშხანის ნაერთები ზოგიერთი თვისებებით ჰგავს ფოსფორის ნაერთებს (რომელიც პერიოდულ სისტემაში იგივე ქვეჯგუფშია). დარიშხანი უფრო ნაკლებად გვხვდება ხუთვალენტიან მდგომარეობაში, უფრო მეტად იგი გავრცელებულია დაჟანგულობის რიცხვით +3. დარიშხანი აგრეთვე ადვილად უკავშირდება თავისთავს მინერალ სკუთერუდიტში. +3 დაჟანგულობის მდგომარეობაში, დარიშხანი ტიპიური პირამიდული ნაერთია, რომელსაც გააჩნია თავისუფალი წყვილი ელექტრონი.
არაორგანული ნაერთები
დარიშხანი წარმოქმნის უფერო, უსუნო კრისტალურ ოქსიდს As2O3 (”თეთრი დარიშხანი”). As2O3, ჰიგროსკოპულია, ადვილად იხსნება წყალში და წარმოქმნის მჟავა ხსნარებს.
დარიშხან (V) მჟავა სუსტი მჟავაა. მის მარილებს არსენიტები ეწოდება, მაგალითად პარიზის მწვანე, კალციუმის არსენატი, რომლებიც სოფლის მეურნეობაში გამოიყენებიან, როგორც ინსექტიციდები და საწამლავები.
დარიშხანის ბევრი ნაერთია ცნობილი გოგირდთან. ასეთებია (As2S3) და (As4S4). ისინი მხატვრობაში გამოიყენება როგორც პიგმენტები. დარიშხანის სულფიდებში As4S3 და As4S10 ჟანგვითი რიცხვია +2 (As4S4).
კარგადაა ცნობილი დარიშხან(III)-ის ტრიფთორიდები, ტრიქლორიდი, ტერიბრომიდი და ტრიიოდიდი, რომელთაგან მნიშვნელოვანია მხოლოდ AsF5. იგი ოთახის ტემპერატურაზე სტაბილურია, მაშინ როცა პენტაქლორიდი სტაბილურია მხოლოდ −50 °C-ზე ქვემოთ.
დარიშხანი როგორც მეთხუთმეტე ჯგუფის ელემენტი გამოიყენება ნახევარგამტარების კომპონენტებად. გალიუმის, ინდიუმისა და ალუმინის არსენიდები გამოიყენება ნახევარგამტარ მასალებად.
ტრიმეთილდარიშხანი
ორგანოდარიშხანის ნაერთები
ორგანოდარიშხანის ნაერთები საკმაოდაა ცნობილი. ბევრი მათგანი I მსოფლიო ომში გამოიყენებოდა, როგორც ქიმიური იარაღი. მათი ზოგადი ფორმულაა R3-xAsClx (სადაც R= ალკილი და არიალია, x= 0,1,2).
კაკოდილ მჟავა ერთ-ერთი პირველი პრაქტიკული ინტერესის მქონე ნაერთია. იგი მიიღება დარიშხანის ტრიქლორიდის მეთილირებით. ამ რეაქციას არა აქვს ანალოგი ფოსფორის ქიმიაში.
მიღება
არსენოპირიტის ჰაერზე დაჟანგვით დარიშხანი სუბლიმირდება დარიშხან (III) ოქსიდად, ხოლო უჰაერო დაჟანგვით ვღებულობთ მეტალურ დარიშხანს.
გამოყენება
დარიშხანი ფართოდ გამოიყენება სპილენძთან და განსაკუთრებით ტყვიასთან შენადნობის სახით. ტყვია გამოიყენება ავტომატურ ბატარეებში, რომელიც საკმაო რაოდენობით შეიცავს დარიშხანს. დარიშხანისა და ტყვიის შენადნობისგან ამზადებენ საფანტს.
სოფლის მეურნეობაში დარიშხანი გამოიყენება როგორც ინსექტიციდი და ფუნგიციდი. ტყვიის წყალბადარსენატმა გამოყენება ჰპოვა ინსექტოფუნგიციდებმა ( ე.ი. მოქმედებს როგორც მწერების, ასევე სოკოების წინააღმდეგ). XX ს-ის ბოლოს მონონატრიუმმეთილარსენატმა (MSMA) და დინატრიუმმეთილარსენატმა (DSMA) - დარიშხანის ნაკლებ ტოქსიკურმა ორგანულმა ფორმამ, სოფლის მეურნეობაში ჩაანაცვლა ტყვიის არსენიტები.
აშშ-ში ცხოველთა ავადმყოფობის პრევენციისა და მათი ზრდის სტიმულირებისათვის, ცხოველთა საკვებს უმატებდნენ დარიშხანს. ამის მაგალითია სოქსარსონი, რომელიც გამოიყენებოდა 1995-2000 წლებში.
XVIII, XIX, XX საუკუნის განმავლობაში დარიშხანის ნაერთები გამოიყენებოდა მედიცინაში. მათ შორის იყო არსფენამინი და დარიშხანის ტრიოქსიდი. ეს უკანასკნელი იხმარებოდა ფსორიაზის წინააღმდეგ. უკანასკნელი პერიოდის კვლევებში მოცემულია ლოკალურ სიმსივნეებში დარიშხან-74 გამოიყენება. დარიშხანი ასევე გამოიყენება საწყის პროდუქტად დარიშხანის პრეპარატების მისაღებად. მისი ზოგიერთი ნაერთი გამოიყენება როგორც სამკურნალო საშუალება.
დარიშხანის შემცველი ნაერთები (As2O3 , KASO2 , Na2HASO4) გამოიყენება სისხლძარღვების დაავადების დროს და ნევრასთენიის შემთხვევაში, აგრეთვე სტომატოლოგიურ პრაქტიკაში და სხვ. დარიშხანის ორგანული ნაერთები (ნოვარსენოლი, მიარსენოლი და სხვა ), ძირითადად იხმარება სიფილისის, მალარიის, ტიფის და სხვა დაავადებების დროს.
სპილენძის აცეტოარსენიტი გამოიყენებოდა როგორც მწვანე პიგმენტი სხვადასხვა სახელწოდებით, მათ შორის ”პარიზის მწვანე” და ”ემერალდის მწვანე”. ცნობილია აგრეთვე ”შეელის მწვანე” (სპილენძის არსენიტი), რომელსაც XIX საუკუნეში ტკბილეულობის შესაღებადაც კი იყენებდნენ.
კალციუმის არსენიდი წარმოადგენს მნიშვნელოვან ნახევარგამტარ მასალას.
დარიშხანს იყენებენ ბრინჯაოში და პიროტექნიკაში. დანიშხანი მცირე რაოდენობით ემატება თითბერს, რომელიც აძლევს მას გამძლეობას, ასეთი თითბერი გამოიყენება წყალგაყვანილობის დანადგარებში. დარიშხანი გამოიყენება ოპტიკურ მინებში, აგრეთვე ტყავის, ბეწვეულის და ფიტულების კონსერვირებისთვის.
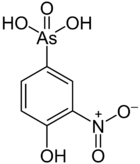
როქარსონი –
ფრინველის საკვების დანამატი
ბიოლოგიური როლი
დარიშხანსა და ფოსფორს შორის მსგავსება იმდენად დიდია, რომ შესაძლებელია ბიოქიმიურ რეაქციებში ფოსფორის ჩანაცვლება დარიშხანით, მაგალითად, ტოქსიკური დოზების ქვემოთ დარიშხანის ხსნადი ნაერთები მოქმედებდნენ, როგორც სტიმულატორები და ეს ნაერთები მცირე დოზებით საკმაოდ პოპულარული იყო XVIIIს-ის შუა წლებში ადამიანებისთვის.
ბაქტერიის ზოგიერთი სახე თავის ენერგიას ღებულობს სხვადასხვა საწვავის დაჟანგვით, რომლის დროსაც არსენატი აღდგება არსენიტამდე. ენზიმები, ცნობილია როგორც არსენატ რედექტაზები.
დარიშხანის ბიომეთილირება. არაორგანული დარიშხანი და მისი შენაერთები, რომლებიც შედიან საკვებში, პროგრესულად მეტაბოლიზდება დარიშხანის ნაკლებ ტოქსიკურ ფორმაში, მეთილირების პროცესების შედეგად. მაგალითად როგორიცაა, მატრიცა Scopulariopsis brevicaulis-ი მნიშვნელოვანი რაოდენობით წარმოიქმნება ტრიმეთილარსენისაგან, თუ იქ არსებობს არაორგანული დარიშხანი. ორგანული ნაერთი - არსენობუტაინი ნაპოვნია წყლის ზოგიერთი საკვებში, როგორიცაა თევზი და სოკო, რომელშიც იგი დიდი რაოდენობითაა. დარიშხანის საშუალო დოზა, რომელსაც ადამიანი ღებულობს, არის 10-650 მგ/ დღეში.
ბანგლადეშსა და მის მეზობელ ქვეყნებში მიწისქვეშა წყლებში დარიშხანის შემცველობამ გამოიწვია მასიური ეპიდემია. დღეისთვის მსოფლიოში დარიშხანის მიწის წყლების მოხმარებისას 42 ძირითადი ინციდენტია აღწერილი. დადგენილია, რომ დაახლოებით 57 მილიონი ადამიანი სვამს დარიშხანის შემცველ წყალს. მის წყლებში, რომელშიც მისი კონცენტრაცია მსოფლიო ჯანმრთელობის ორგანიზაციის სტანდარტებზე მეტია (10 ნაწილი მილიარდზე).
მასალა მომზადებულია www.wikipedia.com -ის მიხედვით



